Joanna Kidoń1, 2, Anetta Lasek-Bal3, 4
1 III Katedra Kardiologii, Śląski Uniwersytet Medyczny w Katowicach, ul. Ziołowa 45-47, 40-635 Katowice, tel. + 48 32 359 87 97 , e-mail: joanna.kidon@sum.edu.pl
2 Dział Fizyki Medycznej, Górnośląskie Centrum Medyczne im. prof. Leszka Gieca Śląskiego Uniwersytetu Medycznego w Katowicach, ul. Ziołowa 45, 40-635 Katowice
3 Katedra i Klinika Neurologii, Śląski Uniwersytet Medyczny w Katowicach, ul. Medyków 14, 40-752 Katowice
4 Oddział Neurologii, Górnośląskie Centrum Medyczne im. prof. Leszka Gieca Śląskiego Uniwersytetu Medycznego w Katowicach, ul. Ziołowa 45, 40-635 Katowice
Streszczenie
Udar mózgu stanowi jedną z wiodących przyczyn niepełnosprawności oraz śmierci na świecie. Pomimo spadku śmiertelności z powodu udaru mózgu, globalne obciążenie udarem wzrasta.
Udar niedokrwienny charakteryzuje niejednorodny patomechanizm, począwszy od obrzęku cytotoksycznego (minuty od wystąpienia incydentu mózgowo-naczyniowego), obrzęku naczyniopochodnego (od 6 godzin), po procesy naprawcze (neuroangiogeneza, neurogeneza) w fazie podostrej i przewlekłej. Do podstawowych technik obrazowania udaru niedokrwiennego mózgu zaliczyć należy przede wszystkim tomografię komputerową (celem wyeliminowania ewentualnego krwawienia, innych przyczyn pogorszonego stanu neurologicznego), rezonans magnetyczny (techniki: dyfuzyjne, saturujące sygnał płynu mózgowo-rdzeniowego, podstawowe, podatności magnetycznej), angiografię (CT, MRI, DSA) oraz ultrasonografię. Techniki dyfuzyjne oraz perfuzyjne (CT, MRI, SPECT, PET) służą do oceny rozległości strefy półcienia. Techniki dyfuzyjne mają szczególne znaczenie w ocenie czasu wystąpienia incydentu mózgowo- naczyniowego. Uważa się, że DWI poprawia wykrywalność udarów niedokrwiennych mózgu aż do 95% w porównaniu ze standardowymi technikami obrazowania. Korelacja map ADC i obrazów DWI pozwala zidentyfikować obszary niedokrwienia. W obrazach DWI sygnał jest hiperintensywny w ciągu kilku minut od incydentu zawałowego, natomiast ADC wykazuje obniżone wartości w czasie od pierwszego do czwartego dnia, w piątej do dziesiątej dobie ma miejsce ich wzrost, po czym następuje wyrównanie względem tkanki zdrowej.
Słowa kluczowe: udar niedokrwienny, obrazowanie MR ważone dyfuzją, DWI, ADC
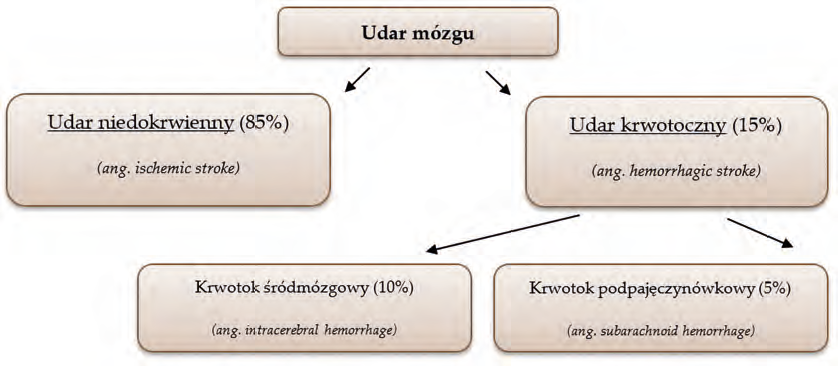
Źródło: Opracowano na podstawie [2].
Udar mózgu
Najważniejszą koncepcją pozwalającą zrozumieć ostry udar i istotę jego leczenia jest stwierdzenie „czas to mózg”. Udar mózgu (incydent mózgowo-naczyniowy) stanowi wiodącą przyczynę niepełnosprawności, a także jedną z wiodących przyczyn śmierci na świecie [1, 2]. W ciągu ostatniej dekady zrewidowano definicję udaru, a także poczyniono znaczne postępy w leczeniu i zapobieganiu udarom. Pomimo spadku śmiertelności z powodu udaru mózgu, globalne obciążenie udarem jednak wzrasta [3]. Zgodnie z danymi opublikowanymi w 2017 r. liczba ludzi na świecie, którzy przeżyli udar wynosi 25,7 miliona [4]. Szacuje się, że częstotliwość pojawienia się nowego incydentu wynosi jeden na 40 sekund oraz że z każdą minutą nieleczonego udaru niedokrwiennego związanego z okluzją dużych naczyń umiera blisko dwa miliony neuronów [2]. Uważa się, że 60% udarów ma miejsce poza szpitalem [3], czyli w warunkach ograniczonego dostępu do pomocy medycznej.
Przyczyną ostrego udaru mózgu jest utrata przepływu krwi, składników odżywczych i tlenu w regionie mózgu, co skutkuje uszkodzeniem neuronów, a w efekcie późniejszymi deficytami neurologicznymi [2]. Dzięki jednak wczesnemu, ukierunkowanemu leczeniu, programom rehabilitacyjnym i długoterminowym zmianom stylu życia można zmaksymalizować szanse na znaczący powrót pacjentów do zdrowia [2].
Udar mózgu definiowany jest jako ogniskowe zmiany neurologiczne o ostrym początku, powstałe z przyczyn naczyniowych [2, 5]. Zasadniczo udar mózgu dzieli się na dwa główne typy: udar niedokrwienny, udar krwotoczny, przy czym pierwszy z nich stanowi najczęściej występujący typ udaru [2, 4]. Rycina 1 zawiera podział udaru mózgu wraz z częstością występowania poszczególnych typów.
Udar niedokrwienny Charakterystycznymi objawami udaru są nagłe, najczęściej ogniskowe deficyty ruchowe i/lub kognitywne (poznawcze). Na podstawie samego obrazu klinicznego trudno jest odróżnić udar krwotoczny od niedokrwiennego. Niewielki krwotok śródmózgowy może objawiać się klinicznie, tak jak rozległy zawał w obrębie półkuli mózgu. Do typowych oznak udaru należy: niedowład połowiczy, opadanie kącika ust, zaburzenia czucia czy też zaburzenia widzenia [6]. U 2-25% pacjentów w pierwszych kilku dniach po udarze niedokrwiennym pojawiają się napady padaczkowe [2]. Oprócz manifestujących się klinicznie udarów, istnieją tak zwane udary nieme klinicznie (tzw. kryptogenne, np. w przebiegu migotania przedsionków). Uwidocznione zostają one w obrazowaniu OUN i mogą być przyczyną zaburzeń kognitywnych oraz spowolnienia psycho-ruchowego [7, 8]. Udar niedokrwienny charakteryzuje się serią zdarzeń patologicznych wywołanych okluzją tętnicy (zmniejszenie CBF1 [9]), która prowadzi do niejednorodnej reakcji patofizjologicznej w różnych fazach: nadostrej, ostrej, podostrej i przewlekłej [5]. Na rycinie 2 zamieszczono poszczególne fazy udaru wraz z najważniejszymi procesami zachodzącymi w poszczególnych fazach.
Przyczynę udaru niedokrwiennego stanowi powstały w naczyniach krwionośnych zakrzep lub zator (np. blaszka miażdżycowa, skupiska bakterii), który może blokować światło naczynia, osadzać się w obrębie wcześniej istniejącego zwężenia, zmniejszać średnicę tętnic w obrębie szyi lub mózgowia czy też pękać [2].
Ważnym celem w diagnostyce udaru niedokrwiennego mózgu jest zdolność do szybkiej i skutecznej identyfikacji rozległości strefy półcienia. Wczesna i dokładna identyfikacja tkanki nerwowej potencjalnie możliwej do uratowania może wpłynąć na identyfikację pacjentów, którzy nadal mogą odnieść korzyści z późnej rekanalizacji (po okresie 6 godzin od pojawienia się incydentu mózgowo- naczyniowego) lub leczenia neuroprotekcyjnego.

Źródło: Opracowano na podstawie [5, 10-12].
Metody obrazowania udaru niedokrwiennego mózgu Do metod obrazowania udaru mózgu (ogniska lub stanu tętnic) zalicza się tomografię komputerową, rezonans magnetyczny, angiografię, a także ultrasonografię. W stanach nagłych tomografia komputerowa bez kontrastu, ze względu na dostępność, czas badania oraz stosunkowo niski koszt, jest najważniejszym pierwszym narzędziem diagnostycznym wykorzystywanym do potwierdzenia diagnozy i wykluczenia krwawienia, udaru krwotocznego czy też innej przyczyny (np. guza) [13, 14]. Rezonans magnetyczny charakteryzuje się bardzo dobrym kontrastem tkankowym, natomiast jego dostępność jest ograniczona, koszt badania jest również wyższy. Angiografia może być wykonana zarówno w oparciu o obrazowanie CT (CTA), MRI2 (MRA), jak i obrazowanie rentgenowskie wiązki stożkowej przy użyciu angiografu (angiografia subtrakcyjna – ang. Digital Subtraction Angiography, DSA). Ta ostatnia pozostaje nadal złotym standardem w ocenie zwężenia światła naczynia, a także stanowi podstawę oceny lokalizacji miejsca mechanicznego udrożnienia naczynia krwionośnego (trombektomii). Ultrasonografia wykorzystywana jest jako badanie dopplerowskie przezczaszkowe głowy oraz naczyń szyjnych, której podstawowym zastosowaniem jest wykrywanie i ilościowa ocena zwężenia naczyń, niedrożności, krążenia obocznego, incydentów zatorowych (mikrosygnałów zatorowych, ang. micro-embolic signals, MES ) [12, 15].
Na podstawie wyniku obrazowania CT i czasu wystąpienia objawów pacjent może być kwalifikowany do leczenia fibrynolitycznego. Obrazowanie MRI ważone dyfuzją wykazuje największą wartość diagnostyczną dla ostrego zawału niedokrwiennego. W celu określenia rozległości strefy półcienia, celem wykonania leczenia reperfuzyjnego w oknie czasowym 4,5-6 godzin, stosuje się obrazowanie perfuzyjne i dyfuzyjne (PWI3/DWI4). Badanie perfuzyjne można wykonać przy użyciu technik tomografii komputerowej, rezonansu magnetycznego czy też technik medycyny nuklearnej: pozytronowej tomografii emisyjnej (obrazowanie PET) oraz tomografii emisyjnej pojedynczego fotonu (obrazowanie SPECT) i polega ono na dynamicznym śledzeniu napływu kontrastu do mózgu. Obrazowanie DWI natomiast mierzy ruch wody w tkance. Jest ono wykorzystywane do wyznaczenia niedokrwionej tkanki, dysfunkcyjnej elektrycznie, która wykazuje ograniczenie dyfuzji (obrzęk cytotoksyczny). Półcień oceniany jest jako obszar niedopasowania (ang. mismatch) obszarów widocznych w PWI i DWI. Należy zaznaczyć, że obszar półcienia zawiera oprócz hipoperfuzyjnie zagrożonej tkanki również taką, która jest w stanie łagodnego i odwracalnego zaburzenia perfuzji (oligemia) i w kontekście terapii pod kontrolą MRI uważana jest za nieistotną i wykluczoną z terapii reperfuzyjnej [12-14, 16-18]. Obrzęk cytotoksyczny, powstały w fazie nadostrej udaru niedokrwiennego, najlepiej widoczny jest w obrazowaniu MRI ważonym dyfuzją i z tego właśnie względu udar niedokrwienny mózgu jest najszybciej widoczny w DWI (w ciągu minuty od wystąpienia incydentu udarowego). Uważa się, że DWI poprawia wykrywalność udarów niedokrwiennych mózgu aż do 95% w porównaniu ze standardowymi technikami obrazowania (CT, MRI bez technik dyfuzyjnych) [12].
Obrzęk cytotoksyczny w tomografii komputerowej bywa trudny do uchwycenia, ponieważ zmiany pochłaniania promieniowania jonizującego (warunkującego kontrast obrazu) są w tym obszarze zbyt subtelne. Obrazowanie dyfuzyjne MRI w postaci sekwencji DWI w udarze niedokrwiennym mózgu zaczyna stanowić złoty standard (zwłaszcza w przypadkach udaru typu wake-up5), natomiast obrazowanie DTI6 wkracza dopiero w tym zakresie w przestrzeń metod diagnostycznych. W literaturze pojawiają się doniesienia naukowe badające przy użyciu sekwencji DTI dynamikę zmian dyfuzji w różnych fazach udaru niedokrwiennego [19], czy też uszkodzenia włókien nerwowych (np. drogi korowo-rdzeniowe, ang. corticospinal tracts, CST) w korelacji z siłą mięśni, predykcji powrotu do sprawności [20, 21].
Cały artykuł dostępny w naszej księgarni. Zapraszamy do prenumeraty lub zakupu bieżącego wydania
WYDANIE 5/2022

